工商時報杜蕙蓉/台北報導
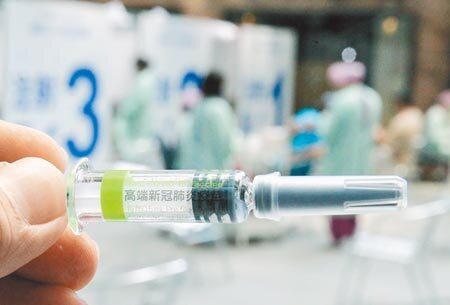
高端(6547)22日公告,經獲歐盟EMA同意後,旗下新冠肺炎疫苗在歐盟的第三期試驗,將規劃以多國多中心方式,與歐盟已上市之新冠肺炎疫苗進行免疫橋接比對試驗,目標盡快取得歐盟認證。
今年6月,由全球主要國家之法規單位所組成的「ICMRA國際藥物監管機構聯盟」,已於會議中達成以免疫橋接進行臨床試驗設計的目標共識。在ICMRA會議之後,日本藥政法規單位PMDA已核准日本第一三共藥廠,以免疫橋接方式執行三期試驗;韓國藥政法規單位MFDS,也核准韓國SK藥廠以3,990人規模,與AZ比較進行三期免疫橋接試驗。
而在日韓核准國內藥廠以免疫橋接執行新冠疫苗三期臨床試驗之前,法國疫苗廠Valneva,已在今年4月21日於英國取得三期IND許可,並在6月3日完成招募4,000名受試者招募,預期今年底Valneva將可取得全病毒去活化新冠疫苗VLA2001與AZ疫苗的免疫橋接三期期中分析數據。
高端表示,經兩個月來與歐盟EMA進行科學諮詢,並取得正面回應後,該公司董事會也通過新冠肺炎歐盟三期免疫橋接試驗初步預算,並確認相關試驗設計原則,後續將依歐盟EMA之科學諮詢結論建議,盡快向EMA提出新冠疫苗第三期臨床試驗申請。
除了EMA試驗外,高端在巴拉圭的臨床試驗也持續進行中,於巴拉圭獨立進行的小型免疫橋椄三期臨床試驗,將用於取得當地臨床資料以進入中南美洲市場。多線同步進行,積極取得國際許可。